羊辞旧岁,金猴迎新。
在这喜迎新春之际,艾德生物再传佳音!我们自主研发的EGFR/ALK/ROS1基因突变联合检测试剂盒已获得国家食品药品监督管理局(CFDA)批准上市(国械注准20163400037),真正为NSCLC临床精准诊疗实现EGFR/ALK/ROS1三基因同步检测!
包括NCCN、ASCO、ESMO以及国家卫计委、抗癌协会等国内外权威机构发布的规范、指南或共识[1-6]均明确指出NSCLC患者在治疗之前应先进行EGFR基因突变和ALK基因融合检测,并建议有条件的单位同时进行ROS1基因融合检测,并根据EGFR、ALK、ROS1的基因状况决定相应治疗策略。
艾德生物系列产品为NSCLC精准诊疗提供简便、快捷的完整检测方案,完全满足临床治疗决策需求
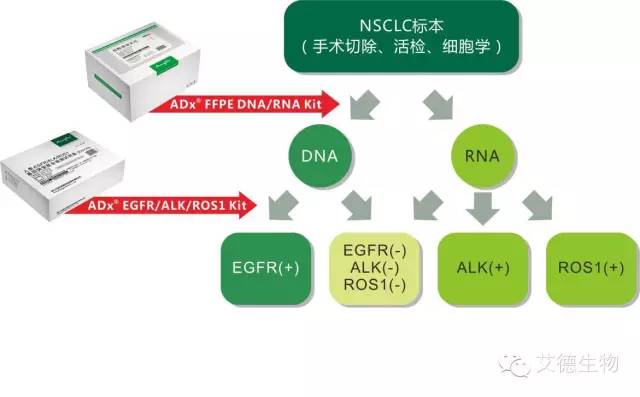
【产品特点】1、 国内唯一获得CFDA批准上市产品;2、 只需1-3片术后组织切片或活检、细胞学等小标本即可满足检测需求;3、 操作简便,6小时即可完成肿瘤组织标本DNA/RNA的同时提取和检测;4、 基于指南及共识推荐的ADx-ARMS和RT-PCR技术平台,判读客观;5、 检测覆盖基因及位点完全满足临床检测需求;6、 适用各型主流PCR仪;
【参考文献】1. NCCN Guidelines, NSCLC, V2.20162. Reck M, et al. Ann Oncol. 20143. Natasha B. Leighl, et al. J Clin Oncol. 20144. 中国原发性肺癌诊疗规范(2015年版)5. 晚期非小细胞肺癌分子靶向治疗专家共识. 20136. 中国间变性淋巴瘤激酶(ALK)阳性非小细胞肺癌诊疗指南,2015