由全国肺癌和病理学领域的多位知名专家共同制定的《非小细胞肺癌血液EGFR基因突变检测中国专家共识》于2015年12月8日在《中华医学杂志》发表。
EGFR突变检测是晚期肺癌患者使用EGFR-TKIs治疗的先决条件。鉴于多种原因,临床实践中EGFR突变的肺癌组织受检率并不高,导致基于驱动基因变异靶点的个体化治疗策略难以实施。多项回顾性和前瞻性研究表明,当肿瘤组织难以获取时,血液循环游离或肿瘤DNA(cf/ct DNA)检测是突变分析合适的替代选择。
中国国家食品药品监督管理局(CFDA)在2015年2月已批准吉非替尼说明书更新,在推荐所有NSCLC患者的肿瘤组织都应进行EGFR突变检测基础上,如果肿瘤组织标本不可评估,则可使用从血液(血浆)标本中获得的ctDNA进行评估。目前我国尚无规范化的血液EGFR突变基因检测的标准或指南。因此,为了规范中国肺癌患者血液EGFR基因突变的检测,特组织全国肺癌和病理学领域的知名专家共同制定本专家共识。
本指南主要包括肺癌的流行病学、EGFR基因突变和EGFR靶向治疗、EGFR组织检测的指南推荐、EGFR的组织检测现状、EGFR血液检测、EGFR突变基因检测报告及周期、血液EGFR基因突变检测发展与展望等8个方面,以下仅为共识中血液EGFR检测部分的内容摘录:
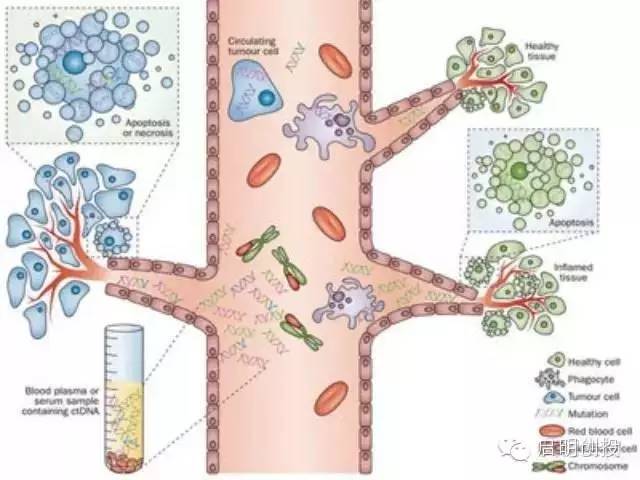
五、EGFR血液检测 研究显示,大部分晚期NSCLC患者的血液中存在循环游离DNA(cfDNA,cell free DNA)。cfDNA主要来源于凋亡或坏死的细胞,包括正常细胞和肿瘤细胞,如果来自肿瘤细胞称为循环肿瘤DNA(ctDNA)。但血液游离DNA片段通常较短,在晚期癌症患者血液中浓度极低,平均约为17微克每升。
既往系列研究(IPASS、IFUM、FASTACT-2)已经在NSCLC患者血液样本ctDNA中发现EGFR基因突变,初步显示外周血ctDNA EGFR基因突变检测及对EGFR-TKIs疗效预测的可行性。
与肿瘤组织相比,ctDNA中EGFR突变检测具有高度特异性(IPASS、IFUM和IGNITE研究中的特异度分别为100%、99.8%和97.2%),但敏感度相对较低(分别为43.1%、65.7%和49.6%),这可能与肿瘤分期、血液标本的处理、检测方法差异等相关。
欧洲药品管理局2014年9月已批准当难以获取肿瘤组织样本时,可采用外周血ctDNA作为补充标本评估EGFR突变状态,以明确最可能从吉非替尼治疗中受益的NSCLC患者。CFDA在2015年2月已批准吉非替尼说明书进行更新,在推荐所有NSCLC患者的肿瘤组织都应进行EGFR突变检测基础上,补充了如果肿瘤标本不可评估,则可使用从血液(血浆)标本中获得的ctDNA进行评估。
血液EGFR基因突变检测的标本采集及处理 为了采集到最佳血浆标本用于后续提取游离DNA进行EGFR突变检测,建议: 1、用含有游离DNA专用保护剂及防细胞裂解保护剂的专用常温采血管采集全血; 2、用常规EDTA抗凝管(严禁使用肝素抗凝管);
考虑到临床实践的方便性,建议尽量采用第一种采集方法,血浆分离时应避免吸入白细胞。
血液EGFR基因突变检测的外周血游离DNA提取 建议采用国家药监部门批准的、大容量血浆游离DNA分离试剂盒。
血液EGFR基因突变检测的方法 目前,检测基因突变最常用的方法是扩增阻遏突变系统(ARMS法),欧盟批准用于指导吉非替尼治疗的血液检测方法也是ARMS检测方法。检测必须在具有资质的检测中心进行。检测方法必须进行严格的验证及质控。检测试剂须使用经CFDA批准的检测试剂盒。
六、EGFR突变基因检测报告及周期 突变检测的报告内容应包括检测结果(建议包括明确的病理诊断及专业的书写)及对结果的诠释,且能够被肿瘤科医师或其他非病理专业的医师理解。其他内容应涵盖患者及标本基本信息、DNA质量、检测方法、检测试剂及仪器、相关临床意义以及在检测过程中出现的状况及不确定结果和因素,以供临床医师全面参考。检测报告模板见附件。
所有专业化EGFR分子检测实验室,通过建立高效率的分子检测平台,优化流程,从接收标本到发出报告周期,建议不超过3~5个工作日,以及时满足临床的需求。
七.血液EGFR基因突变检测发展与展望 不同血浆游离核酸EGFR基因突变检测方法各有优势和劣势,但目前成熟且最常用的检测血液EGFR基因突变的方法是ARMS法,检测敏感度在65%-75%,特异性在98%-100%。数字PCR方法也具有较高的灵敏度,但目前报道的该方法检测EGFR基因突变位点相对有限(19外显子缺失,21号外显子L858R突变以及20号外显子T790M突变),仍处在摸索累积经验阶段,其对操作人员和环境均有较高的要求,未来应用于临床尚需大规模临床数据验证。以二代测序技术(NGS)为代表的新技术拓展了基因突变检测的深度和广度,但其临床转化应用需要更多的数据积累。
八、总结 当肿瘤组织难以获取时,血液是EGFR基因突变检测合适的替代生物材料,也是对可疑组织检测结果的补充。
信息来源:中华医学杂志《非小细胞肺癌血液EGFR基因突变检测中国专家共识》
基于ARMS技术平台,艾德生物研发生产了ADx-ARMS® EGFR基因突变检测试剂盒,并于2011年获得国家食品药品监督管理局(CFDA)批准,上市4年,是目前国内唯一一个可用于临床血液EGFR检测的ARMS法检测试剂盒。
艾德生物专注于精准医疗行业,致力于肿瘤个体化分子诊断技术的创新研发和高端分子诊断产品的产业化。
截止目前,艾德生物已有EGFR、KRAS、NRAS、BRAF、PIK3CA、EML4-ALK、ROS1、ALK/ROS1、KRAS/NRAS、KRAS/NRAS/BRAF、KRAS/NRAS/BRAF/ PIK3CA十一种目前在肿瘤个体化分子诊断领域最重要的基因突变检测产品率先获得CFDA《医疗器械注册证》和欧盟CE认证,同时推出非小细胞肺癌检测套餐和结直肠癌检测套餐可一次性检测非小细胞肺癌和结直肠癌中多个肿瘤驱动基因的变异状态,使肿瘤患者真正从精准医疗中获益。
依靠雄厚的研发实力、优越的产品性能,艾德生物与海峡两岸多家知名医院,阿斯利康、辉瑞、安进等跨国药企建立了战略合作关系,产品已在在40多个国家和地区销售。
未来,艾德生物将和中国的临床专家和病理专家更紧密地合作,为中国的分子诊断提供更好的服务。