2016年6月4日,第52届美国临床肿瘤学会(ASCO)年会上公布了一项名为OO12-01的克唑替尼针对东亚人群的Ⅱ期、开放、单臂临床试验研究数据,证实了ROS1阳性晚期NSCLC患者对克唑替尼的高反应率,达到了试验主要目标。

该临床试验共入组了来自中国、日本、韩国的129例患者,是迄今为止规模最大的ROS1阳性NSCLC研究。其中127名患者接受了克唑替尼治疗,63%的病例到数据截止时(最后一名患者入组后6个月仍在继续服药。由IRR评估的ORR 为69%(95% CI:61-77),第8周的疾病控制率(DCR)达84%,第16周达76%,数据截止时反应仍在持续,中位缓解持续时间(DOR)未达到。该结果证实东亚ROS1阳性晚期NSCLC患者可从克唑替尼治疗中获益。
艾德生物自主研发生产的ROS1融合基因检测试剂盒作为唯一伴随诊断试剂,用于筛选入组该临床试验的ROS1阳性患者,是我国首个肿瘤药物临床试验伴随诊断试剂,艾德生物也成为我国首个参与大型肿瘤药物临床试验的诊断试剂企业。
2016年3月,FDA已批准克唑替尼用于治疗ROS1阳性的晚期NSCLC。此次OO12-01试验结果的发表再次证实了ROS1可作为克唑替尼治疗的新靶点,且该数据更有针对性的证实了克唑替尼在东亚人群ROS1阳性患者中的治疗有效性。ROS1成为继EGFR、ALK之外NSCLC又一明确的治疗靶点。
基于这三个基因的重要治疗意义,国内外权威指南共识均已建议NSCLC在治疗前应明确EGFR、ALK、ROS1三个基因状态,考虑到晚期NSCLC标本有限性,在患者允许下,推荐同时对EGFR、ALK、ROS1三基因进行检测,从而也为临床制定最优化治疗决策节省宝贵时间。
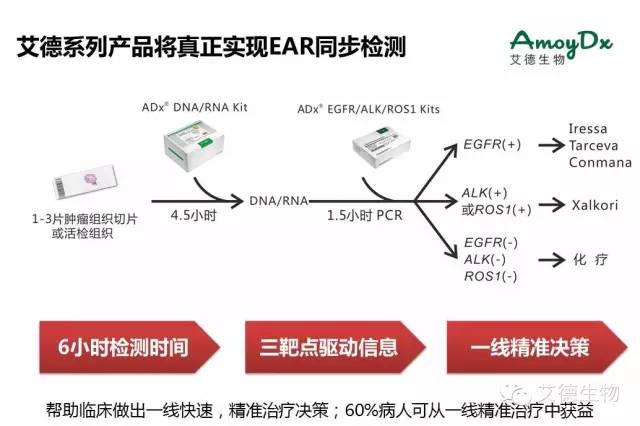
今年1月,艾德生物全新产品EGFR/ALK/ROS1基因突变联合检测试剂盒也获得CFDA《医疗注册证》,是国内唯一获批可同时检测EGFR、ALK、ROS1三基因的试剂产品,为NSCLC临床诊疗真正实现三基因同步检测!