
日前,厦门艾德生物医药科技股份有限公司自主研发的国内首个结直肠癌基因检测套餐-KRAS/NRAS/BRAF/PIK3CA基因突变联合检测试剂盒(可同时一次性检测KRAS、NRAS、BRAF、PIK3CA四个基因状态)获得国家药监局(CFDA)《医疗器械注册证》(国械注准20153401124),填补了市场空白。
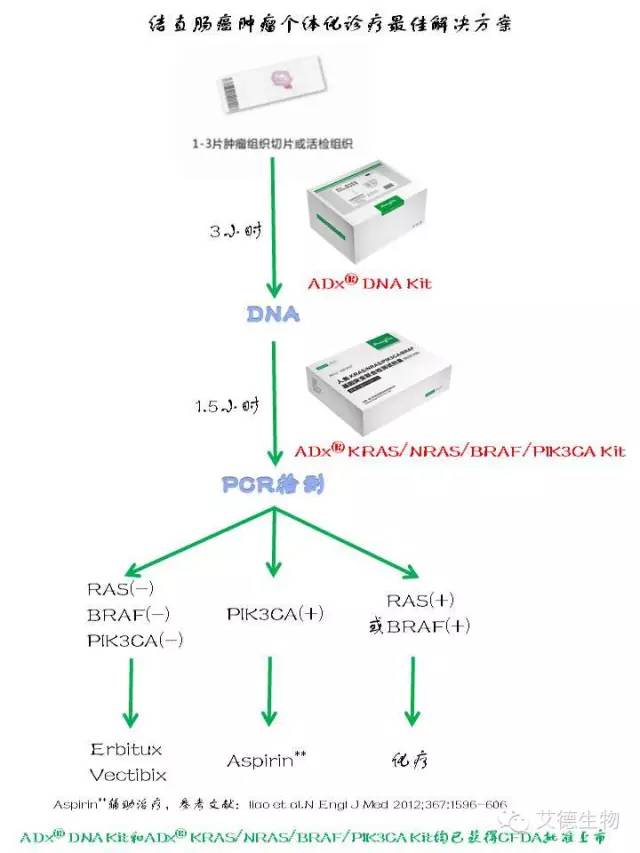
艾德生物为您制定结直肠癌肿瘤个体化诊疗最佳解决方案,KRAS/NRAS/BRAF/PIK3CA基因突变联合检测试剂盒采用临床认可的高灵敏度的ARMS技术,只需1-3片结直肠癌肿瘤组织切片或活检组织,可在4.5小时内完成对肿瘤组织标本的提取和检测,适用于主流的各型PCR仪。
同时,艾德生物的KRAS基因突变检测试剂盒(可检测KRAS外显子2、3、4上的19种KRAS基因突变类型)和NRAS基因突变检测试剂盒(可检测NRAS外显子2、3、4上的16种NRAS基因突变类型)均同时获得国家药监局(CFDA)《医疗器械注册证》(国械注准20153401126和国械注准20153401125)和欧盟CE认证。
美国国立综合癌症网络(NCCN)临床实践指南(1,2)明确指出,RAS基因状态是预测靶向药物爱必妥(ERBITUX®,默克雪兰诺)和Vectibix® (panitumumab,安进)等抗EGFR治疗的重要生物标志物,KRAS/NRAS全部阴性的转移性结直肠癌(mCRC)患者可以从抗EGFR治疗中有更好的生存获益;而BRAF 突变的转移性结直肠癌的预后较差(1,2);Tabernero 博士(3)的一项多中心 I 期研究表明,BRAF抑制剂+抗EGFR治疗+PIK3CA抑制剂的结直肠癌联合治疗生存获益与标准治疗相比较可以使患者的无病生存延长2倍。
参考文献:
1.NCCN Guidelines Version2.2015- Colon cancer
2.NCCN Guidelines Version2.2015- Rectalcancer
3. Cancer Discovery February 2015 5; 102.doi:10.1158/2159-8290.CD-NB2014-186
关于艾德
厦门艾德生物医药科技股份有限公司是专业化的肿瘤个体化分子诊断产品研发及生产企业,致力于肿瘤个体化分子诊断技术的创新和高端分子诊断产品的产业化,是细分市场的领先企业。
公司研发的ADx-ARMS®技术拥有完全自主知识产权,是目前国际上个体化分子诊断领域最先进的技术之一,达到行业公认的国际领先水平。基于核心技术,艾德生物已研发出20余种肿瘤个体化分子诊断产品,其中EGFR、KRAS、NRAS、BRAF、EML4-ALK、PIK3CA、ALK/ROS1、ROS1、KRAS/NRAS/BRAF/PIK3CA九种目前在肿瘤个体化分子诊断领域最重要的基因突变检测产品率先获得CFDA《医疗器械注册证》和欧盟CE认证。目前,艾德产品已在市场大规模销售,涵盖国内大多数三甲医院和40多个国家和地区。